كلورات البوتاسيوم
كلورات البوتاسيوم هو مركب كيميائي يتكون من عناصر البوتاسيوم والكلور والأكسجين، وصيغته الكيمائية هي KCIO3. يوجد المركب في الشروط القياسية على شكل بلورات بيضاء اللون عديمة الرائحة.
| كلورات البوتاسيوم | |
|---|---|
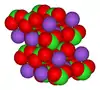 كلورات البوتاسيوم |
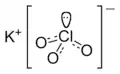 كلورات البوتاسيوم |
 كلورات البوتاسيوم | |
| المعرفات | |
| CAS | 3811-04-9 |
| بوب كيم | 6426889 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| الخواص | |
| الصيغة الجزيئية | KClO3 |
| الكتلة المولية | 122.55 غ/مول |
| المظهر | بلورات بيضاء |
| الكثافة | 2.32 غ/سم3 |
| نقطة الانصهار | 356 °س |
| نقطة الغليان | 400 يتفكك |
| الذوبانية في الماء | 8.15 غ/100 مل ماء عند 25 °س |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
التحضير
يحضر المركب على نطاق صناعي وفق طريقة الكيميائي يوستوس فون ليبيغ، والتي تعتمد على تمرير غاز الكلور في معلق هيدروكسيد الكالسيوم الساخن، ثم بإضافة كلوريد البوتاسيوم إلى المزيج:[2]
يمكن أن يحضر كلورات البوتاسيوم بكميات صغيرة من تفاعل عدم تناسب في محلول هيبوكلوريت الصوديوم، يليه تفاعل تبادل مع كلوريد البوتاسيوم:[3]
كما يمكن أن تتم عملية التحضير من تمرير غاز الكلور في محلول ساخن من البوتاس الكاوي:[4]
الخواص
يوجد المركب في الشروط القياسية على شكل بلورات بيضاء اللون، ذات انحلالية جيدة في الماء الدافئ والساخن.
لكلورات البوتاسيوم خواص مؤكسدة، ويؤدي تسخينه إلى حدوث تفاعل أكسدة-اختزال على نفس المركب (تفاعل عدم تناسب):
أما الاستمرار بالتسخين فيؤدي إلى تفكك المركب:
الاستخدامات
للمركب عدة تطبيقات منها استخدامه في:
- تحضير الأكسجين.
- صناعة أعواد الثقاب.
- صناعة المتفجرات والألعاب النارية.
- يستخدم في الزراعة.
مراجع
- معرف بوب كيم: https://pubchem.ncbi.nlm.nih.gov/compound/6426889 — تاريخ الاطلاع: 19 نوفمبر 2016 — العنوان : 3811-04-9 — الرخصة: محتوى حر
- Реми, Г. Курс неорганической химиию, т. 1/Перевод с немецкого под ред. А. В. Новосёловой. Москва:Мир, 1972.- с. 770//(translated from:) Heinrich Remy. Lehrbuch der anorganischen Chemie. XI Auflage. Band 1. Leipzig:Geest & Portig K.-G., 1960.
- Anne Marie Helmenstine, Ph.D. "Potassium Chlorate Synthesis (Substitute) Formula". About.com Education. مؤرشف من الأصل في 17 فبراير 2017. اطلع عليه بتاريخ 09 يوليو 2015. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, (ردمك 0-07-049439-8)
- بوابة الكيمياء